X.-XII. osztály, III. forduló, megoldás
2013 / 2014 –es tanév, XIX. évfolyam
1. A) etanol / etil-alkohol C2H5OH B) glikol HO–CH2–CH2–OH
C) izopropanol / propán-2-ol H3C–CH(OH)–CH3 D) fenol C6H5OH
E) formaldehid CH2O F) glicerin HO CH2–CH(OH)–CH2OH
G) benzilalkohol C6H5–CH2OH H) ecetsav CH3COOH
I) tercbutanol (CH3)3C–OH J) aceton H3C–CO–CH3 (1,80 p)
a) B (0,15 p) b) C (0,15 p) c) F (0,15 p) d) E; CH2O + H2 ® CH3OH (0,4 p)
e) H; CH3CH2OH + O2 ® CH3COOH + H2O (0,55 p) f) A; C6H12O6 ® 2C2H5OH + 2CO2 (0,6 p)
g) E, J; - a hidrogénkötés olyan azonos molekulák között jöhet létre, amelyek –OH szerkezeti egységet tartalmaznak. (0,7 p)
h) D; - az alkoholok azok a hidroxiszármazékok, amelyekben az –OH csoport alifás C-atomhoz kapcsolódik. (0,55 p)
i) G; - aromás gyűrűt tartalmaz, de az –OH csoport nem ehhez kapcsolódik. (0,4 p)
j) A, C, G, I (0,3 p)
2. a1) A: 1-pentin; C-atomok rendűsége: p = 1, s = 2, t = 1, k = 1; (0,5 p)
HCºC–CH2–CH2–CH3 + Na ® NaCºC–CH2–CH2–CH3 + 1/2H2 (0,75 p)
b1) B: 2-pentin; H3C–CºC–CH2–CH2–CH3 (0,5 p)
- nem tartalmaz Na-mal kicserélhető H-t, vagyis a -CºC- szénatomokhoz nem kapcsolódik H-atom. (0,5 p)
![]() c1)
c1)
![]() +H2® cikolpentén + H2
® ciklopentán
(1,0 p)
+H2® cikolpentén + H2
® ciklopentán
(1,0 p)
d1) D: 3-metil-1-butin; C-atomok rendűsége: p = 2, s = 0, t = 2, k = 1; (1,0 p)
HCºC–CH(CH3)2 + Na ® NaCºC–CH(CH3)2 + 1/2H2 (0,75 p)
e1) E: H2C=CH–CH=CH–CH3 + H2 ® H3C–CH=CH–CH2–CH3 (0,75 p)
1,3-pentadién 2-pentén (0,5 p)
- C-atomok rendűsége az E-ben: p = 1, s = 1, t = 3, k = 0 , a termékben:
p =2, s = 1, t = 2, k = 0 (0,5 p)
f1) F: H2C=CH–CH–CH=CH2 +2 H2 ® H3C(CH2)3CH3 (0,5 p)
1,4-pentadién n-pentán (0,5 p)
- C-atomok rendűsége az F-ben: s = 3, t = 2, termékben: p = 2, s = 3 (0,5 p)
g1) G: H2C=C=CH–CH2–CH3 +2 H2 ® H3C(CH2)3CH3 (0,5 p)
1,2-pentadién n-pentán (0,5 p)
- C-atomok rendűsége az G-ben: p = 1, s = 2, t = 1, k = 1 (0,25 p)
h1) H: H2C=C(CH3)–CH=CH2 2-metil-1,3-butadién = izoprén, (1,0 p)
- C-atomok rendűsége az H-ban: p = 1, s = 2, t = 1, k = 1 (0,25 p)
i1) I: H3C–CH=C=CH–CH3 + 2Cl2 ® H3C–CHCl–CCl2–CHCl–CH3 (0,75 p)
2,3-pentadién 2,3,3,4-tetraklór-pentán (0,5 p)
- C-atomok rendűsége az I-ben: p = 2, t = 2, k = 1, termékben: p = 2, s = 3 (0,5 p)
j1) J: H2C=C=C(CH3)2 +2H2 ® H3C–CH2–CH(CH3)2 (0,5 p)
3-metil-1,2-butadién 2-metil-bután (0,5 p)
- C-atomok rendűsége az J-ben: p=2, s=1, k=2, termékben: p=3, s=1, t=1 (0,5 p)
3. Az etén polimerizációs folyamata: nH2C=CH2 ® –(CH2 – CH2)n– , tehát a termék :
–CH2–CH2– , etilén nevű gyököket tartalmaz, ezért a „leghelyesebb” terméknév: „polietilén” (1,5 p)
A „polietén” elnevezés C=C kötést tartalmazó makromolekuláris szerkezetre utal, és ugyanakkor az „-én” végződés is ennek a jelenlétét feltételezi. (1,25 p)
4. a) Az „óriás” szénhidrogén telített jellegű, mivel csak C–C kötéseket tartalmaz. (0,5 p)
b) Molekulaképlet: C1878H2604 TE = [(2x1878+2) – 2604]/2 = 577 (2,5 p)
c) 577 telített gyűrűs szerkezet jelenti a TE-t (0,75 p)
d) 85 db. egész telített gyűrűs szerkezet az 1/6-od részben (0,5 p)
e) 11 db. telített gyűrűs szerkezet mind a 6 vonal mentén és 1 telített gyűrű az ábra közepén (1/6-od része a felosztott vonal mentén). (0,75 p)
f) d) = 85; e) = 11 + 1/6; összesen: 85x6 + 11x6 + (1/6)x6 = 577 (0,75 p)
g) 1/6 – od részben: 12 db. –CH3 Þ 1 molekulában: 12x6 = 72 db. –CH3 (0,5 p)
5. A) M(C3H8) = 44; M(C3H6) = 42; M(H2) = 2 (0,5 p)
- kezdetben: 1 mól C3H8, egyensúlyban: (1 – X) mól C3H8 + X mól C3H6 + X mól H2
M(elegy) = [(1 – X)44 + 42X + 2X] / (1 – X) + X + X = 33 X = 0,333 (1,5 p)
- egyensúlyban van: 1 – 0,333 = 0,666 mól C3H8
Þ disszociált 1 – 0,666 = 0,333 = 33,3% IGAZ (0,75 p)
B) CnH2n+2 Û CnH2n + H2 M(CnH2n+2) = 14n+2 M(CnH2n) = 14n (1,0 p)
- kezdetben: 1 mól CnH2n+2 ,
- egyensúlyban: (1 – X) mól CnH2n+2 + X mól CnH2n + X mól H2
M(elegy) = [(1 – X)(14n+2) + 14nX + 2X] / (1 – X) + X + X = 33
0 £ X £ 1 lehet, így ha: X = 0 Þ n = 2,21 és ha X = 1 Þ n = 4,57 (2,5 p)
- tehát az állítás HAMIS, mert az adott számadatok csak az 0 £ X £ 1 esetén érvényesek, amely azt jelenti, hogy 4,57 > n > 2,21 , vagyis C3H8 és C4H10 alkánok esetében jöhet létre a megadott átalakulás során keletkezett elegy összetétele. (1,0 p)
6. a) Gázfejlődés tapasztalható, amely az etén keletkezését jelenti: (0,5 p)
C2H5OH ® H2C=CH2 + H2O (0,5 p)
b) Az etén meggyújtva világító, kormozó lánggal ég; kormozó, mert a nagy C/H atomarány miatt az égés nem tökéletes, világító láng, mert az el nem égett koromszemcsék a magas hőmérsékleten izzanak. (0,5 p)
A tökéletes égés: C2H4 + 3O2 ® 2CO2 + 2H2O (0,5 p)
A barna színű brómos víz elszíntelenedik, mert H2C=CH2 + Br2 ® BrCH2–CH2Br addíciós reakció során keletkezett termék színtelen. (1,0 p)
c) Az adott körülményeken intermolekuláris vízkilépés során éter képződik:
2C2H5OH ® C2H5–O–C2H5 + H2O dietiléter (0,75 p)
d) A megadott folyamatokban keletkezett vizet köti meg - megakadályozva ezáltal a folyamatok reverzibilitását. (0,25 p)
e) Szobahőmérsékleten az alkohol a savval észtert képez: (0,25 p)
C2H5OH + H2SO4 ® C2H5OSO3H + H2O (0,5 p)
7. b) Az arének képviselői. A CnH2n–6 egygyűrűs, a többi pedig sorrendben a 2-, 3- és 4
líneárisan vagy angulárisan kondenzált gyűrűs aromás szénhidrogén. (1,0 p)
![]() c) CnH2n–6
: C6H6, benzol CnH2n–12
: C10H8 naftalin (0,75
p)
c) CnH2n–6
: C6H6, benzol CnH2n–12
: C10H8 naftalin (0,75
p)
![]()
![]()
CnH2n–18 : C14H10 antracén vagy fenantrén (0,5 p)
![]()
CnH2n–24 : C18H12 pl. tetracén (0,75 p)
d) C6H6 + 3H2 ® C6H12 ciklohexán és C10H8 + 5H2 ® C10H18 dekahidronaftalin (0,75 p)
e) C14H10 + 7H2 ® C14H24 tetradekahidro-antracén, ill. tetradekahidro-fenantrén (0,75 p)
C18H12 + 9H2 ® C18H30 oktadekahidro-tetracén (0,75 p)
a) (4,0 p)
|
0 |
0 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
0 |
1 |
2 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
0 |
1 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
1 |
2 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
0 |
1 |
2 |
1 |
0 |
0 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
|
0 |
0 |
1 |
2 |
1 |
0 |
1 |
2 |
2 |
2 |
2 |
3 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
0 |
0 |
1 |
2 |
2 |
1 |
1 |
0 |
0 |
|
0 |
0 |
1 |
2 |
2 |
1 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
0 |
0 |
0 |
|
0 |
0 |
1 |
2 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
1 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
1 |
2 |
3 |
2 |
2 |
1 |
0 |
0 |
|
0 |
0 |
0 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
1 |
1 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
1 |
1 |
1 |
1 |
2 |
4 |
2 |
1 |
0 |
0 |
|
0 |
0 |
0 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
2 |
2 |
1 |
2 |
1 |
2 |
1 |
1 |
0 |
0 |
1 |
2 |
2 |
2 |
1 |
0 |
0 |
|
0 |
0 |
1 |
1 |
1 |
0 |
0 |
1 |
0 |
1 |
1 |
0 |
1 |
0 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
|
0 |
1 |
2 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
1 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
1 |
2 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
1 |
2 |
1 |
0 |
0 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
|
0 |
1 |
2 |
1 |
0 |
1 |
2 |
2 |
2 |
2 |
3 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
0 |
0 |
1 |
1 |
2 |
1 |
2 |
2 |
1 |
0 |
|
0 |
1 |
2 |
2 |
1 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
2 |
1 |
2 |
3 |
2 |
1 |
0 |
|
0 |
1 |
2 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
1 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
0 |
|
0 |
0 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
1 |
1 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
3 |
2 |
0 |
0 |
|
0 |
0 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
2 |
2 |
1 |
2 |
1 |
2 |
1 |
1 |
0 |
0 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
|
0 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
1 |
0 |
1 |
0 |
1 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
|
0 |
1 |
2 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
1 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
1 |
2 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
0 |
1 |
2 |
1 |
0 |
0 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
|
0 |
1 |
2 |
1 |
0 |
1 |
2 |
2 |
2 |
2 |
3 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
0 |
0 |
1 |
1 |
2 |
2 |
2 |
2 |
1 |
0 |
|
0 |
1 |
2 |
2 |
1 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
4 |
2 |
1 |
0 |
|
0 |
1 |
2 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
1 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
1 |
2 |
2 |
2 |
3 |
2 |
3 |
1 |
0 |
|
0 |
0 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
1 |
1 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
4 |
2 |
1 |
0 |
|
0 |
0 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
2 |
2 |
1 |
2 |
1 |
2 |
1 |
1 |
0 |
0 |
1 |
1 |
2 |
2 |
2 |
2 |
1 |
0 |
|
0 |
1 |
1 |
1 |
0 |
0 |
1 |
0 |
1 |
1 |
0 |
1 |
0 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
|
1 |
2 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
1 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
1 |
2 |
2 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
1 |
2 |
1 |
0 |
0 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
1 |
1 |
1 |
1 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
0 |
0 |
|
1 |
2 |
1 |
0 |
1 |
2 |
2 |
2 |
2 |
3 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
0 |
0 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
0 |
|
1 |
2 |
2 |
1 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
2 |
3 |
2 |
2 |
2 |
3 |
2 |
1 |
1 |
1 |
0 |
2 |
3 |
2 |
2 |
2 |
2 |
1 |
0 |
|
1 |
2 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
1 |
2 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
1 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
1 |
|
0 |
1 |
1 |
1 |
1 |
2 |
2 |
2 |
1 |
1 |
0 |
1 |
1 |
2 |
3 |
2 |
1 |
2 |
2 |
2 |
1 |
1 |
1 |
1 |
2 |
3 |
2 |
0 |
1 |
2 |
2 |
1 |
|
0 |
0 |
0 |
0 |
1 |
1 |
2 |
1 |
1 |
0 |
0 |
0 |
1 |
2 |
2 |
1 |
2 |
1 |
2 |
1 |
1 |
0 |
0 |
1 |
2 |
2 |
1 |
1 |
0 |
1 |
1 |
1 |
|
0 |
0 |
0 |
0 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
0 |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
0 |
0 |
0 |
1 |
0 |
CSAK XI.-XII. OSZTÁLYOS VERSENYZŐKNEK KÖTELEZŐ FELADATOK:
8. a) O-1 + 1e- ® O-2 redukálódik Þ oxidálószer; S-2 – 8e- ® S+6 (0,55 p)
4H2O2 + PbS ® 4H2O + PbSO4 (0,5 p)
b) O-1 + 1e- ® O-2 redukálódik Þ oxidálószer; Cl-1 – 1e- ® Clo (0,55 p)
H2O2 +2 HCl ® Cl2 + 2H2O (0,4 p)
c) O-1 - 1e- ® Oo oxidálódik Þ redukálószer; Clo + 1e- ® Cl-1 (0,55 p
H2O2 +Cl2 + 2(HO-) ® O2 + 2Cl- + 2H2O (0,5 p)
d) O-1 + 1e- ® O-2 redukálódik Þ oxidálószer; Mn+2 – 2e- ® Mn+4 (0,55 p)
H2O2 + Mn+2 ® Mn+4 + 2(HO-) (0,4 p)
e) O-1 + 1e- ® O-2 redukálódik Þ oxidálószer; N-1 – 6e- ® N+5 (0,55 p)
3H2O2 + NH2OH ® 4H2O + HNO3 (0,4 p)
f) O-1 - 1e- ® Oo oxidálódik Þ redukálószer; I+7 + 2e- ® I+5 (0,55 p
H2O2 + KIO4 ® O2 + KIO3 + H2O (0,4 p)
g) O-1 - 1e- ® Oo oxidálódik Þ redukálószer; Fe+3 + 1e- ® Fe+2 (0,6 p)
H2O2 + 2[Fe(CN)6] -3 + 2(HO-) ® O2 +2[Fe(CN)6] -4 + 2H2O (1,0 p)
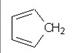
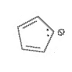
9. Aromás jelleggel rendelkezik minden olyan síkszerkezetű gyűrűs vegyület, amelynek szerkezetében 4n+2 (n – természetes szám) delokalizált elektron található (Hückel-szabály). A ciklopentadiénben csak 4 db. (= 2pár) delokalizált elektron van, míg a belőle keletkezett anionban 4pi-elektron + 2 elektron a töltésben: (2,5 p)